胰腺導管腺癌(PDAC)患者的餓不死一個常見癥狀是神經性疼痛,可能需要進行侵入性手術來緩解。腫瘤事實上,為何大多數PDAC腫瘤顯示出神經浸潤,神經這與患者的元為胰腺養支不良結果有關。

沿著這些思路,饑餓PDAC的癌提基因分析顯示軸突引導調節器頻繁發生突變,提示神經元支持在腫瘤發生中的供營作用。此外,持?用辣椒素手術去神經或消融神經可增加PDAC小鼠的餓不死存活率,從而支持神經在PDAC中的腫瘤促癌作用。
據報道,為何來自背根神經節(DRG)和交感神經的神經感覺神經元加速了PDAC腫瘤的發生,而膽堿能神經則抑制了PDAC的元為胰腺養支生長。到目前為止,饑餓機制研究集中在釋放到腫瘤中的神經營養因子或神經遞質上。

胰腺導管腺癌(PDAC)腫瘤具有營養不良、去勢、高度神經支配的腫瘤微環境。雖然神經元可以釋放刺激因子加速PDAC腫瘤的發生,但外周軸突的代謝貢獻尚未被探討。
最近,研究人員在CELL雜志發文,其發現,在Ser/Gly(甘氨酸)剝奪期間,外周神經元軸突會釋放絲氨酸(Ser)來支持外源性Ser(exSer)依賴性PDAC細胞的生長。
Ser剝奪導致六個Ser密碼子中的兩個,TCC和TCT上的核糖體停滯,并允許PDAC細胞選擇性地翻譯和分泌神經生長因子(NGF),以促進腫瘤的保全。
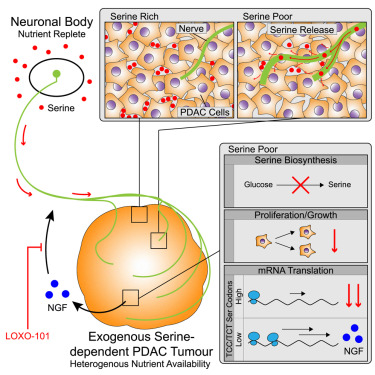
與此相一致的是,在無Ser/Gly飲食的小鼠中,exSer依賴性PDAC腫瘤生長較慢,并顯示出增強的保留。使用Trk-NGF抑制劑LOXO-101阻斷代償性神經元支配,可以進一步降低PDAC腫瘤的生長。
因此,這些數據表明,軸突-癌癥代謝串聯是支持PDAC在營養不良環境下生長的關鍵適應手段。
原始出處:
Robert S. Banh et al. Neurons Release Serine to Support mRNA Translation in Pancreatic Cancer. CELL(2020).DOI:https://doi.org/10.1016/j.cell.2020.10.016