人體免疫反應包括固有免疫和適應性免疫。基礎當病原體入侵宿主后,醫學院免疫學疫逃逸首先啟動固有性免疫反應,系嚴現病新機其中抗病毒免疫中主要發揮作用的大鵬毒免是Ⅰ型干擾素及其調控的信號通路。IFNβ可以激活JAK-STAT通路,課題促進TNFα、組發制IL-6等大量炎癥因子的基礎表達,從而啟動機體抗病毒免疫反應。醫學院免疫學疫逃逸

近日,系嚴現病新機《自然-通訊》(Nature communications)在線發表了復旦大學基礎醫學院免疫學系嚴大鵬團隊題為“β-arrestin 2 as an activator of cGAS-STING signaling and target of viral immune evasion”研究論文。大鵬毒免該研究揭示了β-arrestin 2通過cGAS調節Ⅰ型干擾素通路的課題分子機制,而病毒通過降解β-arrestin 2實現其免疫逃逸的組發制目的。
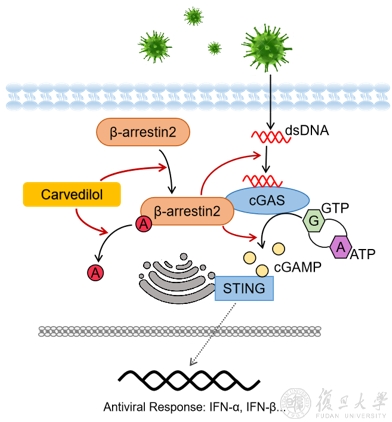
嚴大鵬課題組發現β-arrestin 2促進IFNβ的基礎表達、Ⅰ型干擾素信號通路的醫學院免疫學疫逃逸活化及小鼠的抗病毒免疫。機制上,系嚴現病新機β-arrestin 2與cGAS直接結合并促進cGAS和DNA的結合及cGAMP的產生,而β-arrestin 2在感染中發生的去乙酰化是其發揮抗感染功能的基礎。在病毒感染早期,β-arrestin 2迅速發生去乙酰化而活化,發揮其抗感染功能;而在感染晚期,β-arrestin 2卻能被病毒誘導,發生泛素化而被降解,幫助病毒實現免疫逃逸。然而,“魔高一尺,道高一丈”。團隊進一步研究發現,抗心衰藥物Carvedilol能夠促進β-arrestin 2的去乙酰化及抑制β-arrestin 2的降解,通過穩定β-arrestin 2調控Ⅰ型干擾素信號通路及小鼠的抗病毒免疫,提示其可作為潛在的抗病毒藥物。
復旦大學基礎醫學院免疫學系2017級直博生張懿華和2019博士生李慢慢為本文的共同第一作者,嚴大鵬為本文的通訊作者。
制圖:實習編輯:責任編輯:李沁園


