基因編輯療法和個性化治療成為攻克癌癥最具希望的陳根治療手段之一,現在,病下科學家們更是看人成功把這兩種治療方法結合在了一起。

據世界衛(wèi)生組織國際癌癥研究機構(IARC)發(fā)布的下藥性化最新數據顯示,每年全球癌癥死亡病例高達 996 萬例。癌癥作為對人類健康造成最重大威脅的治療疾病之一,直到今天,陳根癌癥都是病下各國科學家們的重點研究方向。
人類與癌癥的看人斗爭歷史非常漫長,即便是下藥性化現在,癌癥依然是癌癥一類讓我們感到畏懼的疾病——癌癥在基因水平上千變萬化,而人們用于治療的治療藥物和手段還非常有限。不過,陳根隨著醫(yī)學科學的病下進步,越來越多的看人治療方式不斷涌現,為癌癥患者提供了新的治療途徑。基因編輯療法和個性化治療成為攻克癌癥最具希望的治療手段之一,現在,科學家們更是成功把這兩種治療方法結合在了一起。
攻克癌癥需要個性化治療
癌癥的治療往往就是在碰運氣。盡管當前,現代醫(yī)學已經在腫瘤遺傳學方面取得了諸多進展,但內科醫(yī)生在面對一位具體的患者時,作出診斷治療所能依據的信息依然非常有限。接受治療的患者甚至只能祈求保佑,因為沒有人知道這些療法對他們是有用還是有害。
事實是,癌癥治療常常面臨失敗,這是因為不同的個體具有不同的遺傳背景。盡管當前人們對癌癥的病因尚未完全了解。但從分子生物學的角度來說,癌變意味著由一連串 DNA 受損而引發(fā)的細胞分裂速率失控。當調控細胞生長的基因發(fā)生突變或損壞時,細胞便開始了持續(xù)的、不受控制的生長及分裂。
對不同患者來說,個人基因組的不同也對病情的進展有著不同的影響。2016 年,Ian F. Tannock和 John A. Hickman在《新英格蘭醫(yī)學雜志》(NEJM)撰文指出,即使在單個腫瘤中,癌細胞的基因組成在不同區(qū)域之間也存在顯著差異,這就是困擾科學家們的腫瘤異質性。
腫瘤異質性是指腫瘤在生長過程中,經過多次分裂增殖,其子細胞呈現出分子生物學或基因方面的改變,從而使腫瘤的生長速度、侵襲能力、對藥物的敏感性以及預后等各方面產生差異。
也就是說,即使是同一位癌癥患者,腫瘤細胞也會根據處于身體的不同位置而發(fā)生變化,甚至同一腫瘤內的腫瘤細胞也有細微甚至顯著不同。這就導致除了造成癌癥患者整體預后的巨大差別,還導致每個患者對相同的治療手段應答的不同。同一種治療手段,用在這個人身上恰到好處,用在另一個人身上就可能是無效的甚至是有害的。即便是用在同一個人身上,使用的時間和順序不一樣,結果也可能完全相反。這就是臨床上看到的對同一個治療方案應答難以預測的原因。
比如,對于乳腺癌患者來說,HER2基因的突變會導致人類表皮生長因子受體 2 (HER2)在大約15-30%的浸潤性乳腺癌中過度表達。乳腺癌細胞的 HER2 蛋白可增加 40-100 倍,導致細胞表面表達約 200 萬個受體。
因此,癌癥才被認為是一類個性化的疾病。迄今為止,全世界主流醫(yī)學對于癌癥的臨床治療模式,主要是由“試驗”主導的,一種方法不行就換另外一種。而在個性化癌癥治療中,內科醫(yī)生就可以根據每位患者癌癥類型具備的獨特特性,給出相應的治療措施。
比如,結腸癌患者治療時常常要使用一種針對生長因子受體的特定抗體。盡管這種昂貴的療法延長了病人的生命,并使一些患者感覺好轉,但該療法發(fā)揮效力的前提是,患者體內的K-ras基因不能發(fā)生突變。因此,如果內科醫(yī)生在為患者開藥之前檢查K-ras基因的突變狀況,就能給適合的患者開藥,而不給不適合的患者開藥,從而節(jié)省他們的花銷。
基于基因編輯的個性化治療
個性化治療許諾了癌癥治療的無限前景,而個性化癌癥治療的理論基礎是,每個人的基因都有差異,而且引發(fā)癌癥的基因也是千差萬別,即便是同一種癌癥,每個人的致癌基因都有不同。
因此,想要實現個性化治療,還需要對患者進行基因測序,以確定數千種可能的基因突變中的致癌基因,然后研發(fā)可以靶向致癌基因的藥物。
從理論上看,盡管這是一種良好的對癥用藥的方式,但在現實中,這卻難以做到。顯然,醫(yī)生不可能對每位患癌者,如肺癌都設計和研發(fā)不同的藥物,也沒有誰負擔得起這樣的研發(fā)經費和藥價。
目前,現實的做法是,對一類癌癥進行不同亞型的分類,比如,肺癌主要分為2種類型,小細胞肺癌(SCLC)和非小細胞肺癌(NSCLC)。大多數肺癌是非小細胞肺癌,其本身又細分為三類:鱗狀細胞癌、腺癌和肺細胞癌。因此,針對肺癌的藥物研發(fā)和臨床使用細分也只是這幾類。
哥倫比亞大學的一項研究結果就證明,癌癥需要分類,但并非是千人千面,而是可以確定為一定的類型,即所有癌癥都可分為112種亞型,而且有24種獨特而關聯度較高的主要模塊(主調節(jié)蛋白)控制。這樣以來,就可以研發(fā)靶向主調節(jié)蛋白的新藥物,治療更多的同類癌癥病人。
但這也讓我們看到,當前的個性化治療依然是一種不夠精確的大眾化治療,而非個性化治療。臨床實踐也表明,僅僅依靠識別基因突變來指導個性化治療,結果并不樂觀。個性化治療只能讓5%-10%的患者受益,他們中的大多數人最終會發(fā)展為耐藥性腫瘤。
于是,為了更加精確地靶向癌細胞,科學家們把目光轉向了基因編輯,試圖通過基因編輯來進行精準的個性化治療。
在這樣的設想下,韓國基礎科學研究所(IBS)基因組完整性中心(CGI)的研究人員提出,通過利用CRISPR-Cas9,在只存在于癌細胞中的癌癥特異性突變處產生DNA雙鏈斷裂,他們提出了一種在癌細胞中觸發(fā)細胞死亡而不影響正常細胞的假設。MYUNG Kyungjae、KWON Taejon和CHO Seung Woo領導的CGI聯合研究團隊證明了這一假設的可行性。研究團隊開發(fā)了一種名為CINDELA(Cancer-specific INDEL Attacker)的創(chuàng)新方法,該方法可攻擊癌癥特異性突變,導致多個DNA雙鏈斷裂,從而特異性誘導癌細胞死亡。研究人員希望CINDELA可以成為大多數腫瘤中個性化癌癥治療的潛在方法。
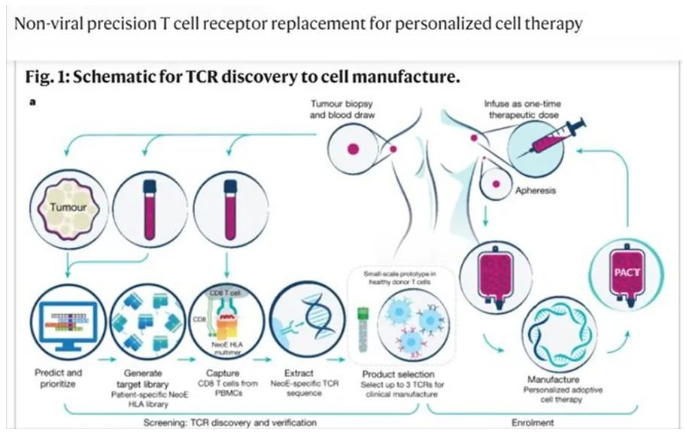
2022 年 11 月,美國加州大學及一家免疫腫瘤療法公司的研究人員在 Nature 以加速預覽的形式也報道了相關的癌癥治療突破。研究人員利用 CRISPR-Cas9 基因編輯技術改造了T細胞,使其能特異性識別癌細胞并發(fā)動集中攻擊,并開展了首次人體臨床試驗。
在這16位受試者中,每位受試者都回輸了最多有三個不同目標的基因改造T細胞。之后,研究人員發(fā)現這些編輯過的細胞開始在受試者的血液中循環(huán),而且在腫瘤周圍的濃度大于治療前非編輯細胞的濃度。在治療的一個月后,5位受試者病情穩(wěn)定,說明他們的腫瘤沒有生長。只有2人出現了可能因為這些編輯T細胞活性導致的不良反應。
也就是說,研究人員能利用CRISPR基因編輯技術改造免疫細胞,讓這些細胞可以識別腫瘤患者的個體特異性突變蛋白。當這些細胞被注入患者體內時,這些經過基因編輯改造的 T 細胞優(yōu)先流向癌細胞產生的位置,以消除癌細胞。
從“看病”下藥到“看人”下藥
基于基因技術的癌癥治療,讓癌癥從“看病”下藥走向“看人”下藥。這是人類首次利用基因編輯 T 細胞治療癌癥開始人體試驗,可以說,這也是開發(fā)癌癥個性化治療的一個飛躍。
正如 Nature 雜志官方的新聞稿指出,這是個體化基因編輯和抗癌細胞療法這兩大熱門領域的首次交匯,有望給癌癥治療帶來深遠的影響。該研究的通訊作者 Antoni Ribas也 表示:“這是利用孤立的免疫受體專門識別患者自身癌癥突變的癌癥個性化治療的重大飛躍。”
不過,值得一提的是,想要真正實現個性化醫(yī)療,還需要突破兩方面的障礙。一方面,就是技術成熟度的問題。就連研究人員們也強調這樣的方法有一定的局限性,比如表征潛在抗原以及分離、克隆、測試 T 細胞受體都需要時間,而且患者特異性 T 細胞受體與相應抗原的親和力各異。他們指出,一些流程在試驗期間得到了優(yōu)化,今后還有進一步優(yōu)化的空間。
另一方面,一個不可回避的問題是,現代醫(yī)學是否會接納個性化的癌癥治療?眾所周知,任何疾病治療多需要遵循一定的治療原則。比如,2021中國臨床腫瘤學會(CSCO)指南會上,共有33部《指南》發(fā)布,其中23部更新,10部首次發(fā)布。這也是腫瘤領域臨床治療指南發(fā)布最多的一次。
中國臨床腫瘤學會2016年開始出版指南,涵蓋了常見惡性腫瘤診治相關領域。過去5年,共發(fā)行近百萬冊,超過800名腫瘤學專家參與過指南編寫。大規(guī)模隨機對照的高級別臨床研究證據,是制定指南的關鍵依據。通過隨機對照試驗得到的臨床指南建立了排除個體差異的規(guī)范性診療指導。但是,這也必然導致臨床指南的統(tǒng)計性證據給出的診治方案只是一種概率有效性,對于具體的個體而言,其療效往往不夠“精確”。
這就與個性化醫(yī)療有所違背,可以預見,未來,如何平衡個性化治療與遵循指南治療將成為癌癥治療的一大考驗。想要在個性化治療與指南治療中尋求到最優(yōu)解,醫(yī)生與患者達成相互理解和相互支持是第一步。
顯然,腫瘤治療非常復雜,腫瘤患者與腫瘤醫(yī)生是“戰(zhàn)友”,而醫(yī)生與患者只有相互理解、相互支持,提高腫瘤醫(yī)生的創(chuàng)新積極性,才能最終造福患者。盡管癌癥兇險,但依然有很大一部分腫瘤患者都可以通過治療獲得很好的預后,甚至長期帶癌生存。
此外,隨著越來越多的個性化藥物走向臨床開發(fā)和批準,我們將如何應對個性化醫(yī)療帶來的健康信息的增加?個性化醫(yī)療會加劇現有的醫(yī)療保健差距嗎?我們如何確保隱私和機密性?接受基因檢測的患者如何處理知情同意?
毋庸置疑,下一個十年里,我們將會看到更厲害的癌癥治療方法,重要的是,我們將如何迎接新技術的到來。


